Welcome to Aso Laboratory
国際化学物理薬学分野 2021年6月〜。
准教授 麻生真理子
生体機能分子化学、蛋白質修飾、核酸関連分子化学
-Research Policy of Laboratory-
Introduction of useful functions and artificial functions into biomolecules, such as nucleic acids,peptides, and proteins, provides new biomolecules, which find a wide range of applications;studying biomolecules,biomaterials, and therapeutics. In our group,several research projects ondevelopment of chemically modified biomoleculeswith useful functions are in progress.
Keywords:Organic Synthesis, Protein modic\fication, Nucleic Acid Chemistry, Bioorganic Chemistry
Reserach Topics
1.機能性核酸分子の設計と合成
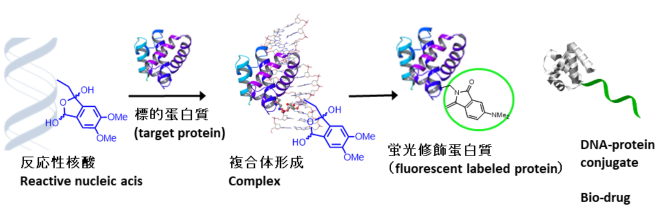
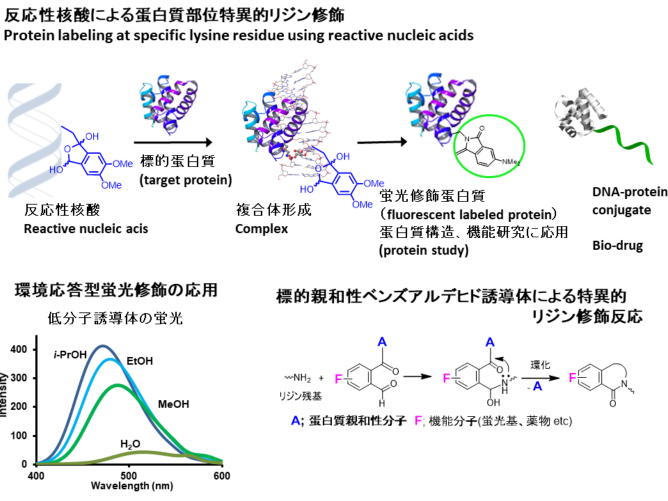
遺伝情報を保持する生体分子である核酸は、たんぱく質や核酸を特異的に認識し、結合する能力を持っています。この核酸に化学反応性(o-ケトベンズアルデヒド誘導体)を付け加えた反応性核酸を設計・合成し、標的とする蛋白質の化学修飾を特異的に行います。例としては蛍光修飾および官能基導入したたんぱく質を得て、標的たんぱく質の構造、機能の理解、制御につなげる研究を行っています。
2. Biodrug創出を目指した生理活性たんぱく質の部位特異的化学修飾安定化、標的化、活性の増強等をもたらすためのたんぱく質の化学修飾は生理活性たんぱく質の医薬化学的応用に有効な方法です。修飾されたたんぱく質が均一な活性を示すには位置やアミノ酸残基特異的化学修飾が重要となります。アミノ酸残基の中でもリシン残基はたんぱく質表面に多く存在しており、良い修飾部位となります。そこで、たんぱく質を特異的に認識する核酸分子にリジン残基を修飾する反応性を組み込み、たんぱく質の部位特異的化学修飾を行う研究を行っています。
(1) Design of nucleic acids with useful functions(2) Site-specific proteinmodification for development of Biodrugs
We design and prepareartificial nucleic acids which modify proteins at specific lysine residue tointroduce usefulfunctions such as fluorescence, and to yieldprotein-conjugate. Obtained modified proteins can be useful forprotein-studiesand as biodrugs.
3.骨病変治療のための医薬分子の創製
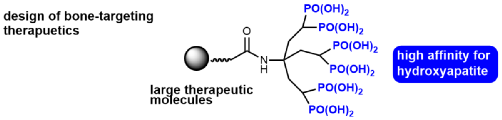
骨は体を支えるだけでなく、体の中で重要な様々な役割を担っています。骨に高い親和性を持つビスホスホネート誘導体を合成し、これを骨粗鬆症をはじめとする骨病変の治療に有効なたんぱく質や、診断に有効な高分子と結合させることで、骨病変に特異的に作用する医薬分子を創り出す研究を行っています。(3) Development ofbone-targeting therapeutic molecules
Bones provide structure for bodies andother important functions. Weworkon development of molecules withhigh bone affinity and its conjugation withtherapeutic proteins for treatment of bone diseases.
共同研究者 阿部由紀子 先生(がんセンター勤務)
連携研究者 田畑香織 先生(九州大学大学院システム創薬分野) 蛋白質研究
【代表論文】
1. C. Gatanaga, B. Yang, Y.Inadomi, K. Usui, C. Ohta, K. Katayama, H. Suemune, M. Aso,
Site-specific turn-on fluorescent labeling of DNA-interacting protein using oligodeoxynucleotides that modify lysine toproduce 5,6-dimethoxy-3-methylene-isoindolin-1-one,
ACS Chem. Biol.8,2216-2221 (2016).
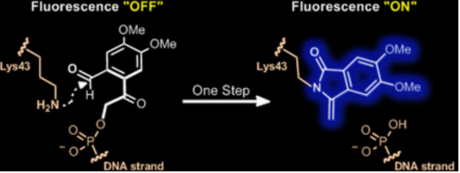
標的蛋白質に結合し、近接するリジン残基を新規蛍光基に変換する反応性を導入したオリゴデオキシヌクレオチドを合成した。新規蛍光基は安定性が高く、修飾蛋白質の解析も容易に進行した。この結果から本手法はDNAと相互作用するタンパク質の蛍光修飾に有用である可能性が示唆された。
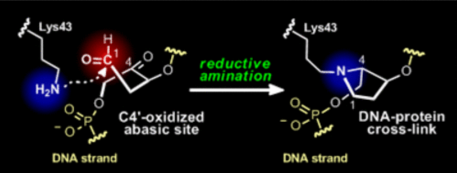
2.B. Yang, A. Jinnouchi, K.Usui, T. Katayama, M. Fujii, H. Suemune, M. Aso,
Bioconjugation of oligodeoxynucleotidescarrying 1,4-dicarbonyl groups via reductive amination with lysine residues,
Bioconjugate Chem.26, 1830-1838 (2015)
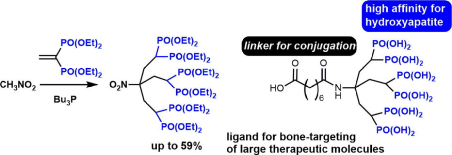
3.K. Shimoda, T. Mitsuoka, K. Ueda, H. Suemune, G. Hirai, M. Aso, Synthesis of dendriticbisphosphonates as bone targetingligands,TetrahedronLett,59, 4528-4531 (2018).
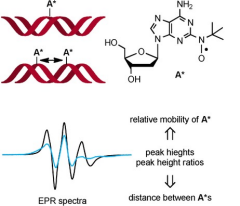
4.M. Kurita, Y. Higuchi, JW Mirc, S. Matsumoto, K. Usui, H. Suemune, M. Aso,Synthesis and electron paramagnetic resonancestudies of oligodeoxynucleotidescontaining 2-N-tert-bututylaminoxyl-2’-deoxyadenosines,ChemBioChem.,17, 2346-2352(2016).
5.Y. S. Abe, S. Sasaki, The adduct formation between the thioguanine-polyamineligands and DNA with the AP site under UVAirradiated and non-irradiatedconditions,Bioorg. Med. Chem.,24, 910-914 (2019).
●大学院生募集
興味のある方は、連絡をお待ちしています。
連絡先
福岡市東区馬出3−1−1 九州大学大学院薬学研究院 麻生真理子
電話 092-642-6877
高 国盛さんが修士1年に入学しました。
2022. 10
薬学部卒業生 権藤さん、佐藤さんが訪問してくれました。
2022. 9
劉 怡萱 さんが薬学修士になりました。
平成4年度修士論文(Master Thesis)
Development of turn-on fluorescentlabeling by converting lysine to stable new environmentsensitivefluorophores-Examination of structure, physicalproperty and reactivity correlation-
2022.7
薬学部卒業生 原田さんが訪問してくれました。
2022.5
高 国盛さんが研究室に参加しました。
2022. 4
王 奕淳さんが研究室に参加しました。
共同研究者 阿部由紀子先生(がんセンター勤務)
連携研究者 田畑香織先生(九州大学大学院)